| Using NMR relaxation for fast Quality Control of Active Pharmaceutical Ingredients
在本案例研究中,一家主要學名藥製造商提供了兩套不同的 API 材料。 第一組包括六批不同的 API,它們以約 20 wt% 的比例預分散在 IsoparG (一種合成的 C10 – C11 異鏈烷烴流體) 中。 所有批次均通過了正常的質量控制測試,該測試基於使用基於雷射散射的設備製備的懸浮液稀釋樣品的平均粒徑測量。
直接對未稀釋的懸浮液測量弛豫時間。 重複性良好 (變異係數 < 1%),因此我們可以得出結論,結果在統計上是穩健的。 根據平均鬆弛時間計算潤濕表面積值 (參見 Mageleka 白皮書 1),結果如 表 1 所示。
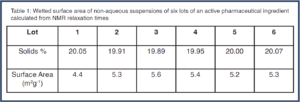
表 1
請注意,對於給定 (固定) 固體濃度,較大的弛豫時間 (馳豫率較小) 通常表示較小的可用潤濕表面積 (較大的顆粒)。 後一個指標直接影響藥物性能,因為根據諾伊斯-惠特尼方程式 (Noyes-Whitney equation),API 的溶出速率由濃度和表面積驅動。
從 表 1 中可以看出,與批次 2、4、5 和 6 相比,批次 #1 的表面積明顯較小 (4.4 m²g⁻¹),批次 #3 的表面積 (5.6 m²g⁻¹) 稍大。 如果有足夠的數據,就可以為質量控制目的定義精確的控制上限和下限。
鑑於了解 API 表面積的重要性 (因為它與生物利用度相關),無需稀釋或其他樣品製備而直接測量潤濕表面積至關重要。 現在可以使用 RelaxoMeter 快速輕鬆地訪問此參數。
由於總表面積主要由任何粒度分佈 (PSD) 的細小顆粒主導 (因為在最簡單的情況下,表面積與粒徑的平方成正比);這表明批次 #1 將具有較少的小顆粒和批次 #3 會分別有更多。 激光散射的局限性在於該技術對 PSD 內的一小部分小顆粒不敏感。 因此,製造商作為正常 QC 提供的 6 個批次的測量平均粒徑不太精確也就不足為奇了。 因此,此處提供的結果強調,僅依賴光散射技術的測量可能會產生誤導並導致錯誤的結論 (請參閱 Mageleka 應用說明 10)。
第二組包含五批以約 13 wt% 分散的 API 水懸浮液。 這些樣品顯然是從不同研磨批次中隨機選擇的。 這裡,QC 標準是使用 Franz 池進行體外釋放測試 (in-vitro release testing; IVRT)。
與之前的研究一樣,潤濕表面積的值是根據直接在未稀釋的懸浮液上測量的平均鬆弛時間計算的。 同樣,NMR 弛豫測量的重複性良好 (變異係數 < 2%),因此我們可以得出結論,結果在統計上是穩健的。 結果如 表 2 所示。

表 2
表 2 中顯示的結果按潤濕表面積增加的順序排列,其值與 IVRT 數據直接相關 (即 API 表面積越大,釋放速度越快)。 鑑於所發現的表面積值的範圍,數據表明懸浮液中的 API 必須使用不同的剪切速率或不同的時間進行研磨。
IVRT 費用昂貴且可能需要相當長的時間。 相比之下,使用 RelaxoMeter 進行的基於 NMR 的測量的速度和簡單性使其成為常規 QC 選擇的理想工具。
| Conclusion
上述示例中的 NMR 弛豫數據展示了 Mageleka RelaxoMeter 如何成為一種快速、簡單的工具,用於對 API 懸浮液的批次間和批次間變化進行質量控制。 RelaxoMeter 基於 NMR 的技術揭示了 API 的根本差異,而傳統 QC 技術 (例如:雷射散射) 無法檢測到,並且比 IVRT 更容易、更便宜且更快。 此外,無需稀釋即可檢測 API 懸浮液的能力為 NMR 弛豫提供了優於其他顆粒表徵技術 (尤其是通過光散射方法進行顆粒測定) 的主要實際優勢。