減小具有不良溶解特性的材料的粒度可以是顯著增加材料總表面積的途徑。 當配製含有活性藥物成分 (API) 的藥物產品時,可以說明這一概念。 更大的表面積允許更快地溶解 API,從而提高生物利用度,無論給藥途徑如何。 這在製造業中顯然很重要,因為藥物的低活性生物利用度會導致治療效率低下和毒副作用的風險。 任何功效的提高都可以降低潛在的毒性,因為需要的原料藥更少,這也有助於降低成本。 還有越來越多的證據表明,特別是納米顆粒 API 材料,顆粒表面積而不是粒徑是控制毒理學相互作用的定義指標。 這解釋了最近基於納米技術開發新配方的動力。
| Case Studies
在以下兩個案例研究中,我們檢查了兩種不同的 API 藥物材料,並展示瞭如何使用 Mageleka MagnoMeter 的 NMR 弛豫測量來實現最佳生物利用度。
第一種 API 是醋酸甲地孕酮,一種天然存在的類固醇激素黃體酮的合成衍生物。 所檢查的樣品是 API 的高級配方,規定為 AIDS 患者使用的食慾增強劑。 它以 12.5 wt% 的濃度作為真正的「納米懸浮液」提供。
使用動態光散射測量的粒度分佈 (PSD) 被發現是均勻的,平均等效球徑為 240 nm。 假設粒子確實是球形的,這將計算出 18 m2 g-1 的表面積。 然而,通過 MagnoMeter 使用 NMR 弛豫直接測量的潤濕表面積被發現為 38 m2 g-1 (圖 1 底部)。 兩種測量技術之間表面積結果的差異出現是因為表面積與直徑的平方趨勢。 NMR 弛豫時間對任何 PSD 中的「細粒」更為敏感 (圖 1 頂部),因此,在此應用中,MagnoMeter 的測量優於動態光散射。 我們可以看到,核磁共振結果表明,略高於 100 nm (大約當前 PSD 的 D10) 的醋酸甲地孕酮粒徑將提供卓越的生物利用度。
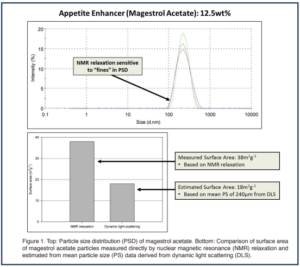
圖 1
第二種原料藥是達匹韋林,一種非核苷類逆轉錄酶抑製劑 (NNRTI),是一種最初開發用於治療 AIDS 的抗逆轉錄病毒藥物。 該材料製備成 10 wt% 的水懸浮液。 API 最初以乾粉的形式生產,粒徑約為 300 µm,但相關材料經過噴射研磨以將粒徑降至 < 10 µm。
使用靜態光散射裝置測得的平均粒徑為 2.4 µm,再次假設為球形,計算表面積為 2 m2 g-1。 然而,使用 NMR 弛豫測量的表面積相當大,為 24 m2 g-1 (圖 2 底部)。 通過檢查 PSD 數據可以很容易地解釋這種差異。 首先,顆粒的顯微照片清楚地表明應該拒絕球形假設 (圖 2 插圖)。 這突出了一個事實,即僅基於光散射技術的粒徑測量可能會產生誤導並導致錯誤的結論。 其次,我們可以看到懸浮液實際上是雙峰的 (圖 2 頂部),如果我們使用較小部分的粒徑,則表面積值是一致的。 這一發現很重要,因為它表明僅 10% 的 API 就佔了 90% 的表面積,因此也就佔了生物利用度、溶出度和細胞毒性。 這再次說明在存在大顆粒的情況下,使用光散射技術測量含有小顆粒或非常小顆粒的懸浮液的表面積的局限性。
在上述兩個案例研究中,結果也說明了使用平均粒徑值計算表面積值的局限性。 任何懸浮液的總表面積將始終由任何 PSD 中較小的尺寸部分決定,這兩個示例都顯示了 NMR 弛豫測量 (例如:來自 MagnoMeter 的測量) 如何在包含納米粒子的懸浮液中提供無偏差的表面積測量。
此外,如果懸浮液中的顆粒不穩定,因此隨著時間的推移有聚集的趨勢,NMR 弛豫測量可以快速檢測到這種效應,因為隨之而來的表面積損失更大。 MagnoMeter 具有專門用於此目的的「時間模式」:它允許連續監測漿液或懸浮液,提供幾乎實時的表面積測量。
使用 MagnoMeter 進行基於 NMR 的測量的速度和簡單性使其成為研發和常規質量控制目的的理想工具。 為了獲得有意義的數據,傳統的光散射技術需要對樣品進行顯著稀釋,因此在獲取用於分析的散裝材料的代表性樣品方面可能存在重大問題。 MagnoMeter 測量任何濃度的懸浮液,因此消除了與獲得代表性採樣相關的代價高昂的錯誤。
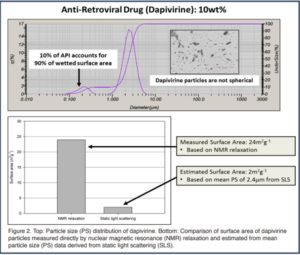
圖 2
鑑於表面積與 API 生物利用度的相關性,快速直接準確測量潤濕表面積,無需稀釋或其他樣品製備,為製藥和醫療保健行業提供了主要優勢。 該指標現在可用於 Mageleka MagnoMeter XRS™。